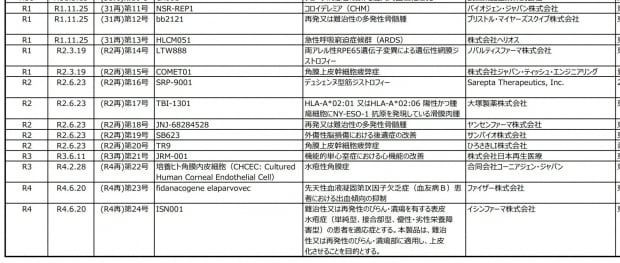
일본 후생노동성 희소질병용 의약품 지정 목록 일부 캡처.
안트로젠(23,100 +0.22%)의 이영양성 수포성 포피박리증 줄기세포치료제(ALLO-ASC-EB, ISN001)가 일본에서 희귀의약품으로 지정됐다.
28일 일본 후생노동성 홈페이지에 따르면 ISN001은 레이와 4년(2022년) 6월 20일 시점에 희귀질환 의약품(희소질병용 의약품) 지정을 받았다. 난치성 또는 재발성의 미란 궤양을 가진 표피수포증의 치료에 대해서다.
안트로젠은 2015년 일본 이신제약에 ALLO-ASC-EB를 기술이전했다. 이신제약은 ISN001이라는 과제명으로 개발해왔다. 이신제약이 후생성에 희귀의약품 지정을 신청했고, 이것이 받아들여진 것이다.
일본에서 희귀의약품으로 지정되면 임상개발 단계에서 후생성 및 의약품의료기구종합기구(PMDA) 등에서 자문을 받을 수 있다. 또 임상개발비의 20%를 세액공제받는다. 우선심사 및 승인심사비 감액, 재심사 기간 최대 10년 연장 등의 혜택이 있다.
이신제약은 현재 일본에서 이영양성 수포성 표피박리증 환자 6명을 대상으로 ISN001의 임상 3상을 진행 중이다. 3상 완료 이후 허가받으면 ISN001의 생산은 안트로젠이 맡는다. 이신제약이 일본 판권을 갖고 있다. 허가 시 단계별기술료(마일스톤)와 상업화 매출에 대한 경상기술사용료(로열티)도 안트로젠이 받게 된다.
안트로젠은 ALLO-ASC-EB의 국내 임상 1·2상을 하고 있다. 성인 환자의 임상을 완료했고, 소아 환자 3명에 대한 임상이 완료되면 당국과의 협의를 거쳐 허가를 신청할 예정이다. 미국에서도 2상을 진행 중이다.
한민수 기자 hms@hankyung.com





